在蛋白降解技术中,基于溶酶体系统开发的靶向蛋白降解技术有哪些?AUTOTAC、第一代、第二代 AUTAC? 你能分清吗?
01
蛋白降解技术
在蛋白降解技术中,目前最具开发潜力的是利用泛素化-蛋白酶体途径的靶向降解技术,其代表技术为 PROTAC。但蛋白酶体系统并不适用于所有蛋白的降解,如与神经退行性疾病相关的蛋白聚集体、较大体积的蛋白或非蛋白靶标,如脂滴等。
除蛋白酶体降解系统之外,溶酶体降解系统也是真核细胞中重要的降解途径。由于溶酶体含有多种酸性水解酶,可降解包括蛋白、核酸、脂质在内的多种物质,很好地补充了蛋白酶体降解系统的不足。
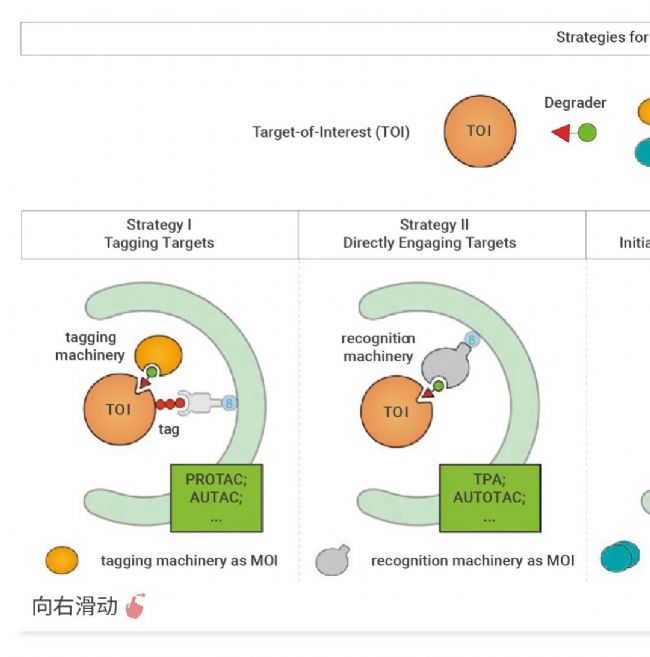
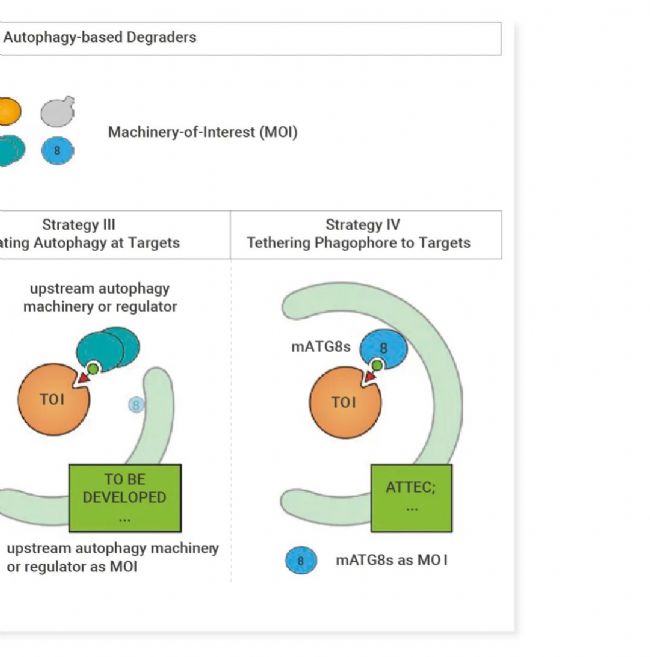
图 1. 基于自噬溶酶体系统开发的自噬依赖靶向降解技术[1]。
目前基于溶酶体系统开发的靶向蛋白降解技术包括AUTAC (AUtophagy-TArgeting Chimera),AUTOTAC (AUTOphagy-TArgeting Chimera),ATTEC (Autophagosome-tethering compound) (详见:ATTEC 分子: 通过自噬降解多靶点的闪亮新星!)等。其中 AUTAC 、AUTOTAC 及 ATTEC 是利用自噬-溶酶体降解机制进行蛋白降解。
第一代/ 第二代 AUTAC & 第二代AUTOTAC
第一代 AUTAC 和第二代 AUTAC 既然都叫 AUTAC,所以降解机制是一样的。
而 AUTAC 和 AUTOTAC 名字虽然很像,但二者从作用机制上还是存在差异的。AUTAC 是诱导底物打上泛素化标签,底物受体通过泛素化标签与底物结合,而 AUTOTAC 是直接将底物与底物受体结合起来。
由于基于自噬溶酶体系统的蛋白降解技术的开发基础是选择性自噬机制,所以首先我们先了解一下选择性自噬的机制。
02
选择性自噬机制
选择性自噬机制主要包括两个过程:底物识别和分离膜招募[1]。其机制如下:
- 底物识别: 底物受体与底物结合,主要有两种方式:(1) 通过降解标签结合:识别机器 (底物受体,支架蛋白等) 结合底物表面的降解标签。(2) 直接结合:识别机器直接与底物结合。
- 分离膜招募: 大部分底物受体都通过结合分离膜表面的 mATG8 蛋白而招募分离膜。除上述机制外,一些底物受体以及支架蛋白还可招募上游自噬机器 (autophagy machinery) 及它们的调节蛋白,例如 ULK1 复合物与 BK1 等,以促进在底物所在位置 (in situ,即原位) 形成分离膜。
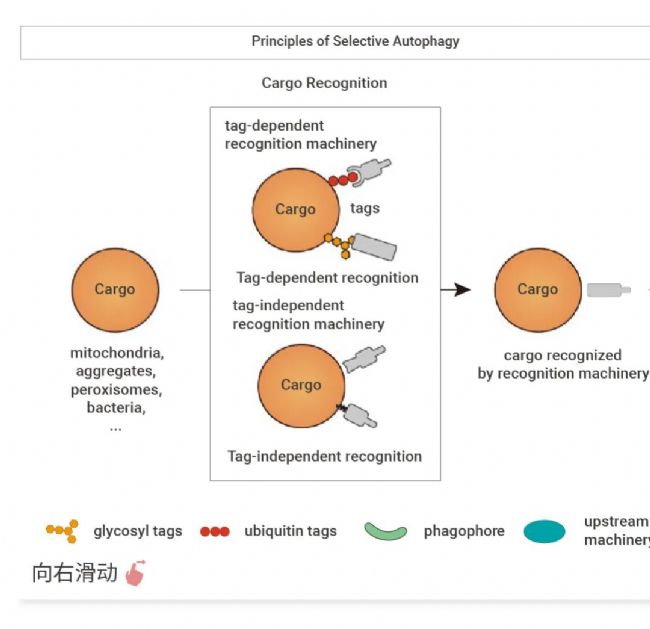
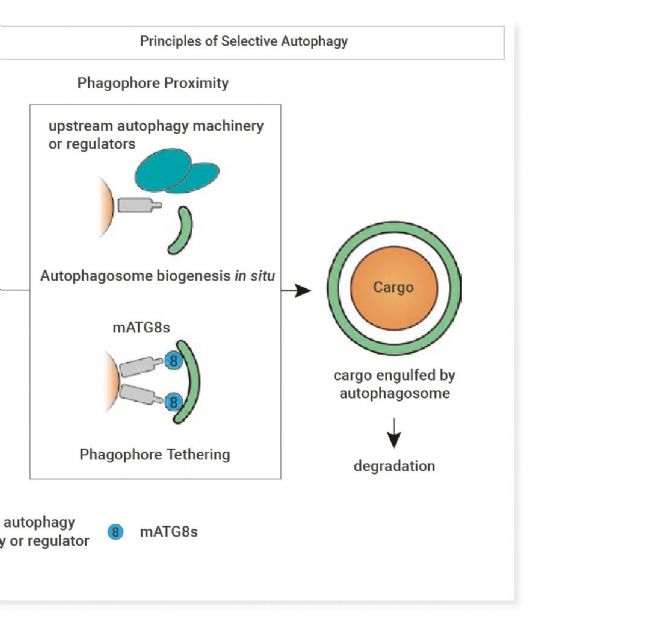
图 2. 选择性自噬作用机制[1]。
03
AUTOTAC
AUTOTAC (AUTOphagy-TArgeting Chimera), 即自噬靶向嵌合体。AUTOTAC 包括三部分:目的蛋白配体、p62 靶向配体以及连接二者的 linker。
AUTOTAC 作用机制:
AUTOTAC 和 p62 的 ZZ 结构域结合,使得原本无活性的 p62 构象被激活诱导为自噬相容形式,暴露出 PB1 和 LIR 结构域,PB1 和 LIR 分别可以促进 p62 与靶蛋白复合物的自聚集及其与自噬膜上 LC3 的相互作用,从而诱导靶蛋白经过溶酶体降解[2]。其中p62就是一种底物受体,AUTOTAC通过将底物与受体连接,实现底物识别,进而被降解,所以AUTOTAC 的机制是介导底物受体与底物的结合,即底物识别中的直接结合机制。
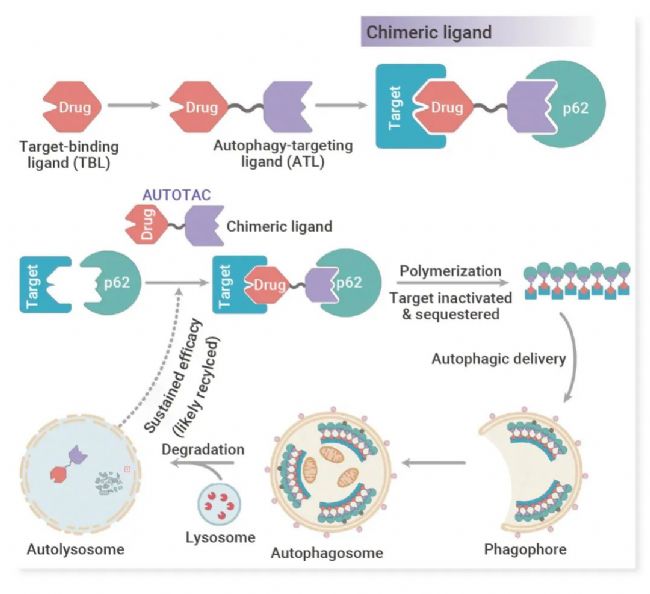
研究表明,利用 AUTOTAC 技术可成功在体外和体内降解神经退行性病变中的癌蛋白和蛋白质聚集体。该技术的可行性为蛋白降解领域提供了一个新的策略。
研究人员首先针对 p62 的 ZZ 结构域进行 3D 建模,然后进行结构和活性研究,最终确定了 YOK-2204、YOK-1304 和 YTK-105 三种化合物,之后通过 PEG linker 将 p62-ZZ 配体和靶蛋白配体连接合成多种 AUTOTAC,并验证了 AUTOTAC 不仅可以介导癌蛋白降解,还可以降解错误折叠蛋白即蛋白聚集体的降解[2]。
与 PROTAC 相比,PROTAC 实现靶蛋白的有效降解和 Linker 长度及类型密切相关,但 AUTOTAC 的效果或许并不特别的依赖于 Linker 的长度,这为 AUTOTAC 设计提供了更多的灵活性[2]。
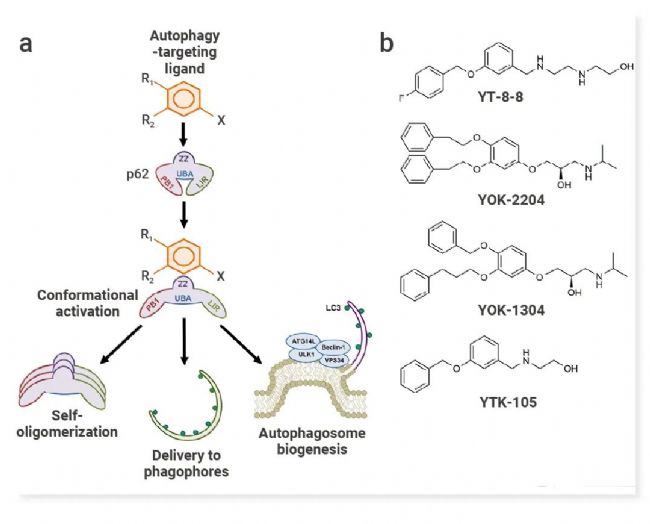
图 4. 自噬靶向配体作用模式的模型 (a) 与自噬靶向配体的化学结构 (b) [2]。
04
AUTAC
AUTAC (AUtophagy-TArgeting Chimera) 主要由 3 部分组成,分别是靶蛋白配体、Linker 和降解标签鸟嘌呤衍生物 (GD)。
AUTAC 的作用原理:通过降解标签模拟 S-鸟苷酸化修饰,诱导靶蛋白的多聚泛素化,即给靶蛋白打上降解标签,识别机器通过降解标签与靶蛋白结合,实现底物识别。所以 AUTAC 机制不同于 AUTOTAC,是借助降解标签实现底物识别。
AUTAC 具有更加广泛的降解范围,不仅可以降解细胞质蛋白,还可以实现降解个头较大的细胞器,包括内质网、线粒体和过氧化物酶体等。
第一代 AUTAC
研究发现,在链球菌自噬清除过程中,S-鸟苷化在多泛素化过程中具有重要机制,然而具体的自噬机制仍然不清楚。基于之前研究背景,第一代 AUTACs 选择鸟嘌呤衍生物 (cGMP) 作为自噬标签来诱导内源性 S-鸟苷酸化。所有报道的第一代 AUTAC 化合物均具有半胱氨酸作为亚结构[3]。
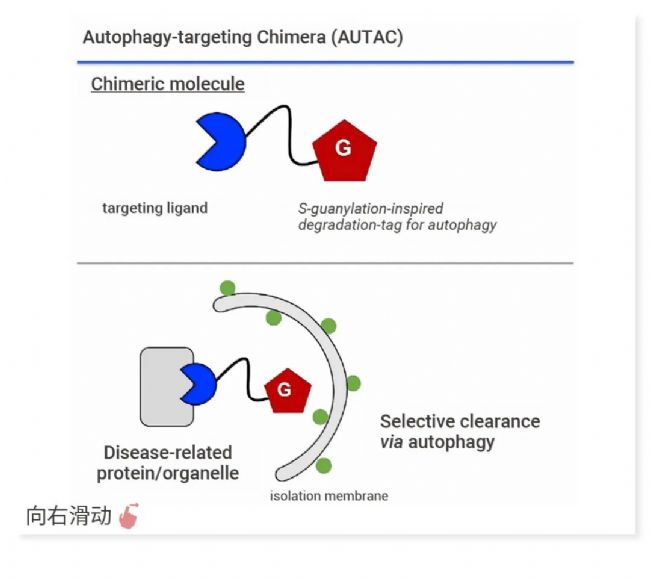
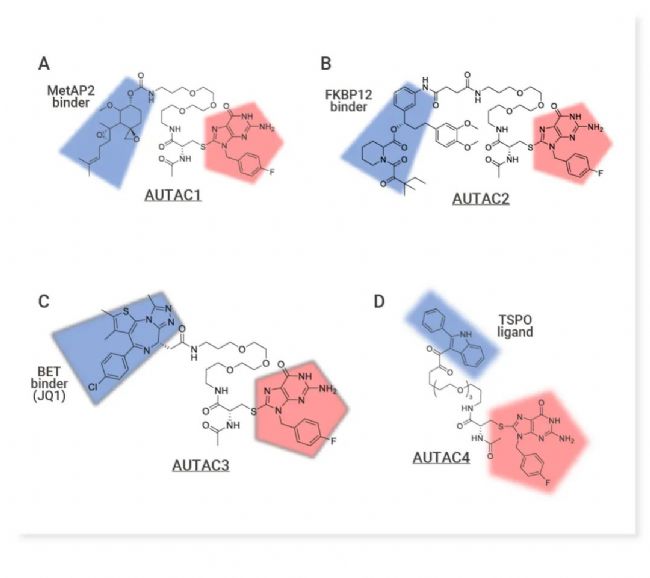
图 5. AUTAC 作用机制 (左) 部分报道的第一代 AUTAC 分子(右) [3]。
第二代 AUTAC
第一代 AUTAC 的开发,主要集中在替代内源性 S-鸟苷化中发现的磷酸化核糖结构,因为 cGMP 的半胱氨酸亚结构会导致不必要的蛋白激酶 G (PKG) 激活。此外,环磷酸的负电荷可能会影响 AUTAC 细胞膜的通透性。
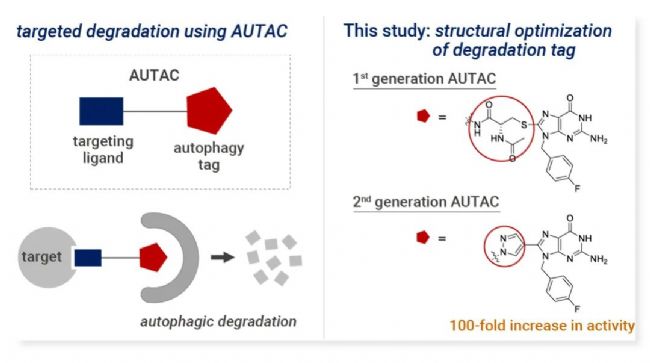
Hirokazu Arimoto 教授团队基于此前研究背景对 AUTACs 进行了结构-活性关系 (SAR) 研究,分别对第一代 AUTAC 鸟嘌呤部位及半胱氨酸部位用不同结构进行替换,发现鸟嘌呤在 AUTAC 中发挥重要作用,而用吡唑环替代半胱氨酸可以明显提高 AUTAC 活性。第二代 AUTAC 与第一代 AUTAC 相比,其活性提高了 100 倍[4]。
05
小结
AUTAC 与 AUTOTAC 都是利用自噬-溶酶体降解机制进行蛋白降解,都是在底物识别阶段介导蛋白降解,但具体的降解机制略有不同,AUTAC 是诱导底物打上泛素化标签,底物受体通过泛素化标签与底物结合,而 AUTOTAC 是直接将底物与底物受体结合起来。
| 产品推荐 |
| YOK-2204 (HY-161738) YOK-2204 是 p62-ZZ 结构域的配体。YOK-2204 可以激活 p62 依赖性的选择性巨自噬。YOK-2204 可用于 AUTOTAC 设计。 |
| YOK-1304 (HY-161739) YOK-1304 是 p62-ZZ 结构域的配体。可以激活 p62 依赖性的选择性巨自噬。YOK-1304 可用于 AUTOTAC 设计。 |
| YTK-105 (HY-W489121) YTK-105 是 p62-ZZ 结构域的配体。YTK-105 可以激活 p62 依赖性的选择性巨自噬。YTK-105 可用于 AUTOTAC 设计。 |
| FBnG-(Cys-acetamide)-CH2-PEG3-CH2-CH2-CH2-NH2 (HY-150408) 第一代 AUTAC 降解标签鸟嘌呤衍生物与 PEG linker 偶联物。 |
| AUTAC1 (HY-134183) AUTAC1 是一种 MetAP2 靶向自噬介导降解体 (AUTAC)。AUTACs 包含一个降解标签和一个弹头确保靶向特异性。AUTAC1 包含一个 FBnG 和一个 Fumagillol 部分。Fumagillol 共价结合到 MetAP2 上。 |
| AUTAC2 (HY-134184) AUTAC2 是一种 FKBP12 靶向自噬介导降解体 (AUTAC)。AUTAC2 包含一个 FBnG 和 SLF 部分,其中 SLF 与 FKBP12 非共价结合。 |
| AUTAC2-2G (HY-163127) AUTAC2-2G 是第二代 AUTAC,活性提高了 100 倍。 |
| Amino-PEG3-2G degrader-1 (HY-158985) 第二代 AUTAC 降解标签鸟嘌呤衍生物与 PEG linker 偶联物。 |
参考文献:
[1] Yiqing Zhang, et al. Manipulating autophagic degradation in human diseases: from mechanisms to interventions. 5 July 2022; Accepted: 8 October 2022. Life Medicine, 2022, Volume 1.
[2] Ji CH, et al. The AUTOTAC chemical biology platform for targeted protein degradation via the autophagy-lysosome system. Nat Commun. 2022 Feb 16;13(1):904.
[3] Takahashi D, et al. AUTACs: Cargo-Specific Degraders Using Selective Autophagy. Mol Cell. 2019 Dec 5;76(5):797-810.e10.
[4] Takahashi D, et al. Second-Generation AUTACs for Targeted Autophagic Degradation. J Med Chem. 2023 Sep 14;66(17):12342-12372.

